Hibridisasi adalah penyetaraan tingkat energi melalui penggabungan antarorbital senyawa
kovalen atau kovalen koordinasi.Teori hibridisasi dipromosikan oleh
kimiawan Linus Pauling dalam menjelaskan struktur molekul seperti metana
(CH4). Secara historis, konsep ini dikembangkan untuk sistem-sistem
kimia yang sederhana, namun pendekatan ini selanjutnya diaplikasikan
lebih luas, dan sekarang ini dianggap sebagai sebuah heuristik yang
efektif untuk merasionalkan struktur senyawa organik.
Teori
hibridisasi tidaklah sepraktis teori orbital molekul dalam hal
perhitungan kuantitatif. Masalah-masalah pada hibridisasi terlihat jelas
pada ikatan yang melibatkan orbital d, seperti yang terdapat pada kimia
koordinasi dan kimia organologam. Walaupun skema hibridisasi pada logam
transisi dapat digunakan, ia umumnya tidak akurat.
Sangatlah penting
untuk dicatat bahwa orbital adalah sebuah model representasi dari
tingkah laku elektron-elektron dalam molekul. Dalam kasus hibridisasi
yang sederhana, pendekatan ini didasarkan pada orbital-orbital atom
hidrogen. Orbital-orbital yang terhibridisasikan diasumsikan sebagai
gabungan dari orbital-orbital atom yang bertumpang tindih satu sama
lainnya dengan proporsi yang bervariasi. Orbital-orbital hidrogen
digunakan sebagai dasar skema hibridisasi karena ia adalah salah satu
dari sedikit orbital yang persamaan Schrödingernya memiliki penyelesaian
analitis yang diketahui. Orbital-orbital ini kemudian diasumsikan
terdistorsi sedikit untuk atom-atom yang lebih berat seperti karbon,
nitrogen, dan oksigen. Dengan asumsi-asumsi ini, teori hibridisasi
barulah dapat diaplikasikan. Perlu dicatat bahwa kita tidak memerlukan
hibridisasi untuk menjelaskan molekul, namun untuk molekul-molekul yang
terdiri dari karbon, nitrogen, dan oksigen, teori hibridisasi menjadikan
penjelasan strukturnya lebih mudah.
Teori hibridisasi sering
digunakan dalam kimia organik, biasanya digunakan untuk menjelaskan
molekul yang terdiri dari atom C, N, dan O (kadang kala juga P dan S).
Penjelasannya dimulai dari bagaimana sebuah ikatan terorganisasikan
dalam metana
a. Hibridisasi sp3
Hibridisasi menjelaskan atom-atom yang berikatan dari sudut pandang sebuah atom. Untuk sebuah karbon yang berkoordinasi secara tetrahedral (seperti metana, CH4), maka karbon haruslah memiliki orbital-orbital yang memiliki simetri yang tepat dengan 4 atom hidrogen.
Konfigurasi keadaan dasar karbon adalah 1s2 2s2 2px1 2py1 atau lebih mudah dilihat:
Hibridisasi menjelaskan atom-atom yang berikatan dari sudut pandang sebuah atom. Untuk sebuah karbon yang berkoordinasi secara tetrahedral (seperti metana, CH4), maka karbon haruslah memiliki orbital-orbital yang memiliki simetri yang tepat dengan 4 atom hidrogen.
Konfigurasi keadaan dasar karbon adalah 1s2 2s2 2px1 2py1 atau lebih mudah dilihat:
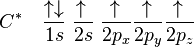
b. Hibridisasi sp2
Senyawa karbon ataupun molekul lainnya dapat dijelaskan seperti yang dijelaskan pada metana. Misalnya etilena (C2H4) yang memiliki ikatan rangkap dua di antara karbon-karbonnya.
Senyawa karbon ataupun molekul lainnya dapat dijelaskan seperti yang dijelaskan pada metana. Misalnya etilena (C2H4) yang memiliki ikatan rangkap dua di antara karbon-karbonnya.
Karbon
akan melakukan hibridisasi sp2 karena orbtial-orbital hibrid hanya akan
membentuk ikatan sigma dan satu ikatan pi seperti yang disyaratkan
untuk ikatan rangkap dua di antara karbon-karbon. Ikatan hidrogen-karbon
memiliki panjang dan kuat ikat yang sama. Hal ini sesuai dengan data
percobaan.
Dalam hibridisasi sp2, orbital 2s hanya bergabung dengan dua orbital 2p:
Dalam hibridisasi sp2, orbital 2s hanya bergabung dengan dua orbital 2p:
c. Hibrid sp
Ikatan kimia dalam senyawa seperti alkuna dengan ikatan rangkap tiga dijelaskan dengan hibridisasi sp.
Dalam model ini, orbital 2s hanya bergabung dengan satu orbital-p, menghasilkan dua orbital sp dan menyisakan dua orbital p. Ikatan kimia dalam asetilena (etuna) terdiri dari tumpang tindih sp-sp antara dua atom karbon membentuk ikatan sigma, dan dua ikatan pi tambahan yang dibentuk oleh tumpang tindih p-p. Setiap karbon juga berikatan dengan hidrogen dengan tumpang tindih s-sp bersudut 180°.
Dalam model ini, orbital 2s hanya bergabung dengan satu orbital-p, menghasilkan dua orbital sp dan menyisakan dua orbital p. Ikatan kimia dalam asetilena (etuna) terdiri dari tumpang tindih sp-sp antara dua atom karbon membentuk ikatan sigma, dan dua ikatan pi tambahan yang dibentuk oleh tumpang tindih p-p. Setiap karbon juga berikatan dengan hidrogen dengan tumpang tindih s-sp bersudut 180°.
